第四回 生成AIは、超小型ゲノム編集ツール開発をどう変えるのか
- コラム
自然探索から、目的指向の分子設計へ
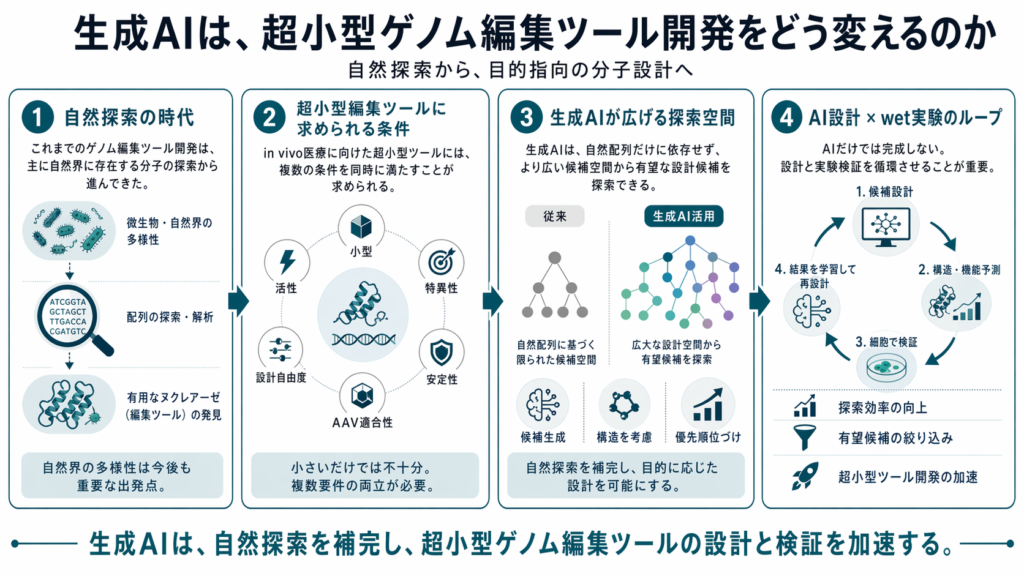
ゲノム編集ツールの開発は、自然界から有用な酵素を探索する時代から、目的に応じて分子を設計する時代へ進みつつあります。その変化を後押ししているのが、タンパク質設計における生成AIの進展です。本記事では、生成AIが超小型ゲノム編集ツール開発にもたらす可能性を整理します。
ゲノム編集ツールの開発は、これまで主に自然界から有用な酵素を探索し、その性質を調べ、必要に応じて改良するという流れで進んできました。CRISPR-Casシステムをはじめ、多くの編集ツールは、微生物が持つ自然の防御システムに由来しています。
この自然探索型のアプローチは、極めて強力です。自然界には、長い進化の過程で生まれた多様な分子機能が存在しており、そこから有用な酵素を見つけることは、ゲノム編集技術の発展に大きく貢献してきました。
一方で、自然に存在する分子が、そのまま人間の医療応用や産業応用に最適であるとは限りません。たとえば、編集酵素のサイズ、標的認識性、PAM/TAM制約、活性、安全性、細胞内安定性、送達適性などは、用途によって求められる条件が異なります。
ここで重要になるのが、目的指向の分子設計 という考え方です。
目的指向の分子設計とは、単に自然界から候補を探すのではなく、「どのような用途に使いたいのか」「どのようなサイズ制約があるのか」「どの標的配列を狙いたいのか」「どのような安全性条件が必要なのか」といった要件から逆算して、分子を設計するアプローチです。
近年、この分子設計を大きく変えつつあるのが、生成AIです。
タンパク質の配列、構造、進化的関係、機能情報を学習したAIモデルは、従来の経験的な変異導入や限定的なスクリーニングでは探索しにくかった分子空間を提案できる可能性があります。特に、タンパク質構造予測、逆フォールディング、配列生成、機能予測、進化的制約の推定などを組み合わせることで、より目的に沿った候補分子を設計することが可能になりつつあります。
超小型ゲノム編集ツールの開発において、生成AIが果たし得る役割は大きく3つあります。
第一に、候補空間の拡張です。自然界に存在する既知配列だけでなく、それらと関連しながらも異なる新しい配列空間を探索できます。これにより、既存の編集ツールとは異なる性質を持つ候補を見出せる可能性があります。
第二に、目的制約を踏まえた設計です。たとえば、構造を大きく崩さずに特定の認識部位を変える、PAM/TAM認識性に関わる領域を設計する、サイズを維持しながら活性や安定性を改善する、といった設計課題に対して、AIは有力な候補を提示する補助ツールになり得ます。
第三に、実験検証の効率化です。分子設計において、すべての候補を実験で試すことは現実的ではありません。AIを用いて候補を絞り込むことで、限られた実験リソースをより有望な候補に集中できます。特にスタートアップや小規模研究チームにとって、実験回数を減らしながら成功確率を上げることは重要です。
ただし、生成AIは万能ではありません。AIが提案した配列が、実際に細胞内で発現し、正しく折りたたまれ、標的DNAを認識し、安全に編集できるかどうかは、最終的には実験で確認する必要があります。したがって、生成AIは実験を置き換えるものではなく、実験の前段階で候補を設計・優先順位づけするための強力な補助技術と捉えるべきです。
重要なのは、AIと実験を分離して考えないことです。AIが候補を設計し、実験がその候補を評価し、その結果を再び設計に反映する。この循環を作ることで、分子開発のスピードと精度を高めることができます。
超小型ゲノム編集ツールの開発は、まさにこのAIと実験の統合が求められる領域です。自然に存在する酵素を出発点にしながら、医療応用に必要な制約から逆算して新しい分子を設計する。そのようなアプローチが、次世代のゲノム編集技術を切り開く可能性があります。
私たちは、生成AIを単なる流行語としてではなく、分子設計の考え方を変える基盤技術として捉えています。自然探索から目的指向の分子設計へ。この変化は、ゲノム編集ツール開発のあり方そのものを変えていくと考えています。


