第五回 超小型ゲノム編集ツールが拓く次世代バイオ医療
- お知らせ
in vivo編集、創薬、疾患モデル、産業基盤への展開
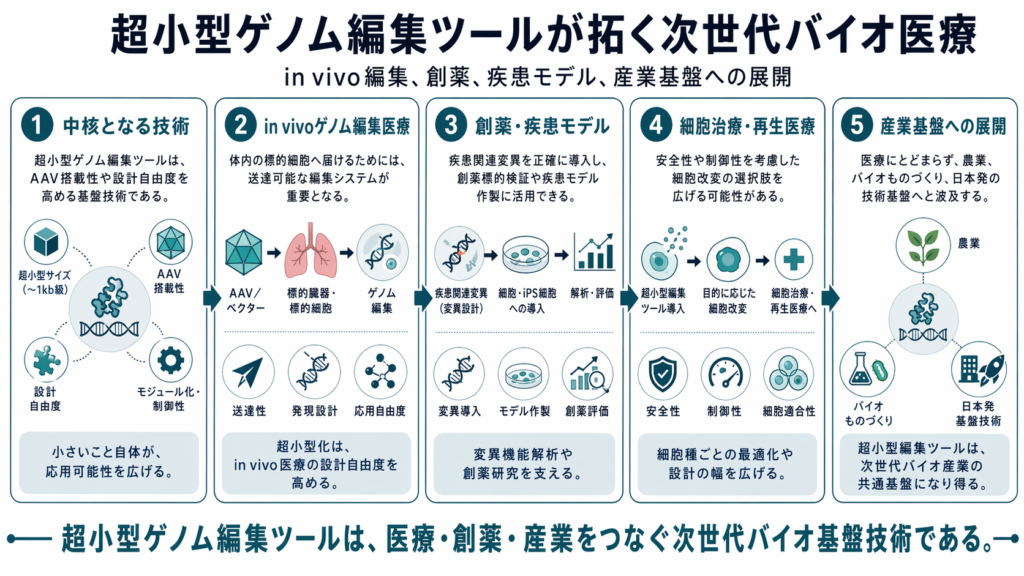
超小型ゲノム編集ツールは、in vivo医療だけでなく、創薬、疾患モデル、産業バイオにも広がる可能性を持っています。送達しやすく、設計自由度の高い編集ツール群は、次世代のバイオ医療基盤になり得ます。本記事では、その応用可能性と今後の展望を整理します。
超小型ゲノム編集ツールは、単に「小さい編集酵素」というだけではありません。送達しやすく、設計自由度が高く、用途に応じた改良が可能な編集ツール群は、次世代のバイオ医療・創薬・研究開発を支える重要な基盤技術になる可能性があります。
特に、TnpBやIscBのような小型RNA誘導型DNA編集酵素は、従来の代表的な編集酵素とは異なる特徴を持つ候補として注目されています。これらの酵素を起点に、自然探索、構造解析、生成AI、実験検証を組み合わせることで、新しい編集ツール空間を開拓できる可能性があります。
超小型ゲノム編集ツールの応用先として、まず重要なのが in vivoゲノム編集医療 です。
患者体内で直接ゲノムを編集する医療では、編集ツールを標的細胞へ届けることが大きな課題になります。AAVなどの送達ベクターを用いる場合、搭載できる分子サイズには制限があります。そのため、より小型の編集酵素は、送達設計上の大きな利点を持ちます。小型化によって、編集酵素、ガイドRNA、発現制御配列などを一つの設計に収めやすくなり、治療設計の自由度が高まる可能性があります。
第二の応用先は、創薬研究です。
創薬では、遺伝子機能の検証、疾患関連変異の解析、標的遺伝子の評価、薬剤応答性の検討などにゲノム編集が活用されます。より多様な編集ツールが利用できるようになれば、従来は編集しにくかった標的や細胞種に対しても、新しい実験系を構築できる可能性があります。
特に、疾患関連変異を細胞モデルに導入し、その機能的影響を評価する研究では、標的配列の制約をどこまで下げられるかが重要です。PAM/TAM制約を調整できる編集ツール群を持つことは、疾患モデル作製や機能解析の自由度を高めます。
第三の応用先は、疾患モデルです。
ヒト疾患の理解には、患者由来細胞やiPS細胞、オルガノイド、動物モデルなどを用いた疾患モデルが重要です。ゲノム編集により、特定の変異を導入したり、疾患関連遺伝子を操作したりすることで、病態の理解や治療法探索が進みます。
より小型で扱いやすい編集ツールが利用できれば、モデル作製の選択肢が広がります。また、複数の編集ツールを用途ごとに使い分けることで、研究開発の柔軟性が高まります。
第四の応用先は、産業バイオ基盤です。
ゲノム編集は、医療だけでなく、農業、食品、環境、微生物生産、バイオものづくりなど、幅広い産業領域に関わります。さまざまな生物種や細胞種で使いやすい編集ツール群を持つことは、産業応用の広がりにもつながります。
また、独自の編集ツール空間を持つことは、事業戦略上も重要です。既存技術を利用するだけでなく、自ら設計・改良したツール群を持つことで、研究開発の自由度、知財戦略、提携可能性が広がります。
もちろん、超小型ゲノム編集ツールの開発には多くの課題があります。編集効率、安全性、標的特異性、細胞内安定性、免疫原性、送達適性など、医療応用に向けて検証すべき項目は多くあります。AIが候補を提案したとしても、最終的には実験による慎重な評価が不可欠です。
しかし、これらの課題があるからこそ、基盤技術としての価値があります。送達制約、サイズ制約、標的制約、知財制約を踏まえながら、新しい編集ツールを設計することは、次世代のバイオ医療に向けた重要な研究開発テーマです。
今後、ゲノム編集技術は、既存ツールを利用する段階から、目的に応じて編集ツールを設計・選択する段階へ進んでいくと考えられます。超小型ゲノム編集ツールは、その変化を支える重要な選択肢の一つです。
私たちは、in vivo編集、創薬、疾患モデル、産業バイオをつなぐ次世代の基盤技術として、超小型ゲノム編集ツールの可能性に注目しています。AIによる設計と実験検証を組み合わせることで、新しいバイオ医療の技術基盤を生み出していきたいと考えています。


