第三回 なぜ独自のゲノム編集ツール空間が重要なのか
- コラム
既存技術に依存しすぎない日本発バイオ基盤技術へ
ゲノム編集は、医療・創薬・産業バイオを支える重要な基盤技術になりつつあります。だからこそ、既存技術を利用するだけでなく、独自の編集ツール空間を持つことが重要です。本記事では、技術的自由度、応用範囲、知財戦略の観点から、その意味を整理します。
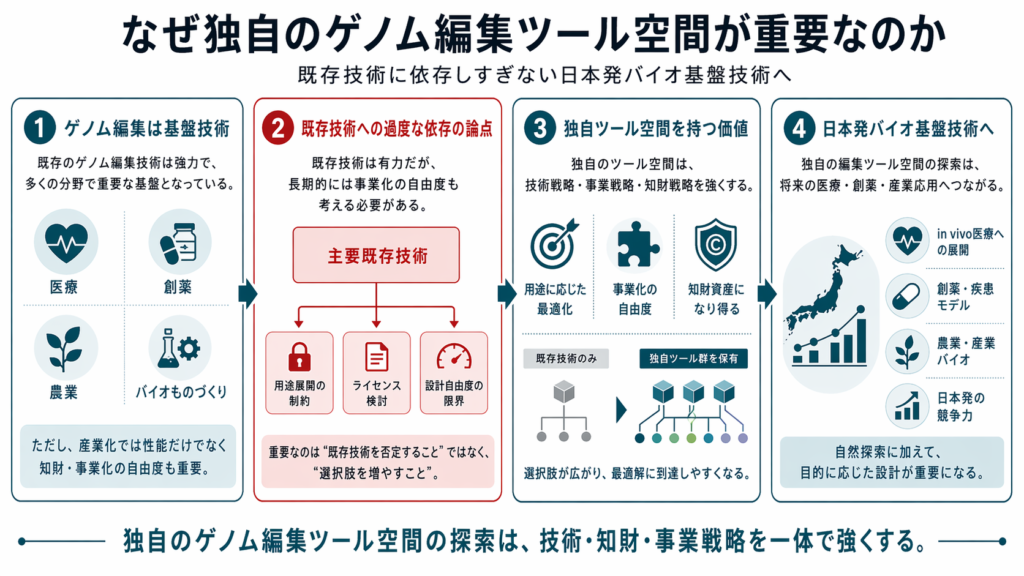
ゲノム編集技術は、基礎研究から医療応用、創薬、農業、産業バイオまで、幅広い領域で重要な基盤技術になっています。特にCRISPR-Casシステムの登場以降、遺伝子を狙って改変する技術は急速に普及し、多くの研究開発を加速してきました。
一方で、今後の産業応用を考えると、既存の代表的な編集ツールだけに依存し続けることには、いくつかの課題があります。技術性能、用途適合性、送達制約、知財、事業上の自由度といった複数の観点から、独自のゲノム編集ツール空間を持つことの重要性が高まっています。
ここでいう「ツール空間」とは、単一の編集酵素だけを指すものではありません。酵素の配列、構造、標的認識性、PAM/TAM制約、サイズ、活性、安全性、送達適性、用途ごとの設計自由度を含む、技術群としての広がりを意味します。
既存の代表的な編集ツールは非常に強力です。しかし、すべての用途に最適とは限りません。たとえば、in vivo医療では、送達ベクターに搭載できるサイズが重要になります。特定の疾患変異を狙う場合には、編集可能な標的配列の制約が問題になります。産業応用では、性能だけでなく、長期的な知財戦略やライセンス自由度も重要になります。
このような背景から、自然界に存在する編集酵素を探索するだけでなく、目的に合わせて新しい編集ツールを設計する取り組みが重要になっています。特に、TnpBやIscBのような祖先型・小型のRNA誘導型DNA編集酵素は、新しい編集ツール空間を開拓する候補として注目されています。
独自のツール空間を持つことには、少なくとも3つの意味があります。
第一に、技術的な自由度です。既存ツールでは対応しにくいサイズ制約、標的制約、送達制約に対して、別の設計解を持つことができます。特に小型編集酵素は、AAV搭載性などの観点から重要な選択肢になり得ます。
第二に、応用領域の拡張です。ゲノム編集の用途は、今後さらに多様化していきます。遺伝性疾患、がん、神経疾患、細胞治療、創薬スクリーニング、疾患モデル作製など、用途ごとに必要な編集ツールの条件は異なります。単一の万能ツールではなく、用途に応じたツール群を持つことが、応用範囲を広げます。
第三に、事業上の独自性です。バイオテクノロジーの基盤技術では、性能と同時に、知財上の自由度が重要です。既存技術の周辺で開発を進めるだけでは、事業化や提携の際に制約を受ける可能性があります。独自の設計空間を持つことは、研究開発上の差別化だけでなく、将来の事業戦略においても重要です。
特に日本においては、海外発の基盤技術を利用するだけでなく、独自のバイオ基盤技術を創出することが重要です。ゲノム編集は、医療、創薬、食料、環境、産業バイオに関わる横断的な技術であり、その基盤を国内から生み出すことは、科学技術戦略上も大きな意味を持ちます。
今後のゲノム編集技術は、単に「既存の酵素を使う」段階から、「目的に合わせて編集ツールを設計する」段階へ進んでいくと考えられます。その中で、自然探索、構造解析、機械学習、生成AI、実験検証を組み合わせることにより、従来とは異なる新しい編集ツール空間を開拓できる可能性があります。
私たちは、既存技術を尊重しつつも、それに過度に依存しない新しい編集ツール群の開発が、次世代のバイオ医療・創薬・産業基盤につながると考えています。


