第二回 AAVに搭載できる超小型編集ツールがなぜ重要なのか
- コラム
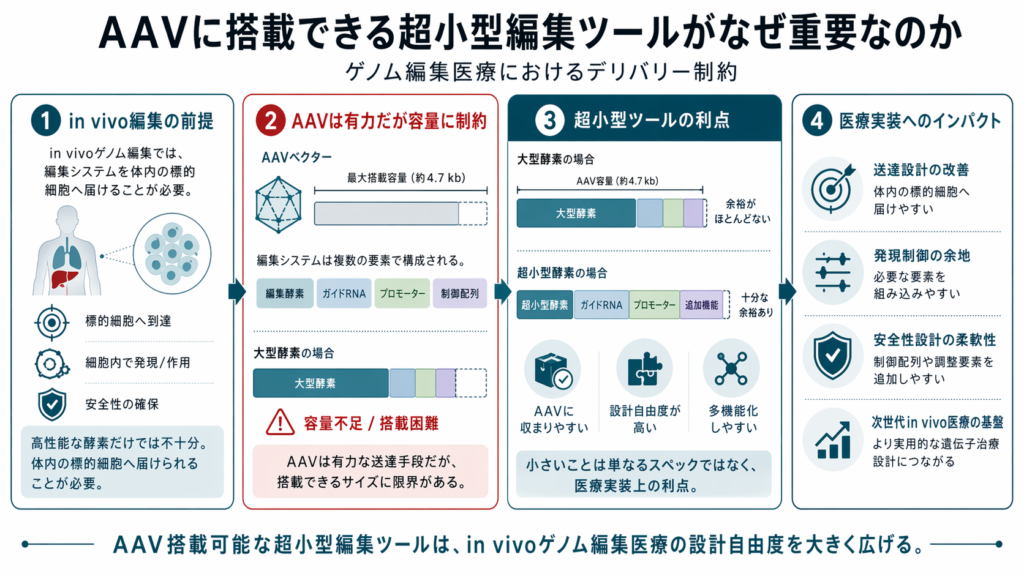
ゲノム編集医療におけるデリバリーの制約
ゲノム編集医療では、編集酵素の性能だけでなく、それを目的の細胞へ届けるデリバリー設計が重要です。特にAAVベクターを用いる場合、搭載できる分子サイズには明確な制約があります。本記事では、AAV搭載性という観点から、超小型ゲノム編集ツールの意義を考えます。
ゲノム編集医療を実現するうえで、編集酵素そのものの性能は非常に重要です。しかし、それと同じくらい重要なのが、編集ツールを体内の目的細胞へ届ける デリバリー技術 です。
特に、in vivoゲノム編集では、患者の体外で細胞を操作するのではなく、体内に編集ツールを投与し、目的の臓器や細胞で機能させる必要があります。この場合、編集酵素がどれほど優れていても、標的細胞に届かなければ治療効果は期待できません。
現在、in vivo遺伝子治療やゲノム編集医療で重要な送達手段の一つが、AAV、すなわちアデノ随伴ウイルスベクターです。AAVは、さまざまな組織への送達実績があり、遺伝子治療の分野で広く研究されてきました。特定の臓器や細胞に対する指向性、比較的長期の発現、臨床応用に向けた知見の蓄積などから、今後も重要な送達プラットフォームであり続けると考えられます。
一方で、AAVには明確な制約があります。その一つが、搭載できる遺伝子サイズの制限です。AAVベクターには、搭載できる配列量に上限があるため、大型の編集酵素をそのまま搭載することは難しい場合があります。さらに、実際の治療設計では、編集酵素だけでなく、ガイドRNA、プロモーター、ポリA配列、制御配列なども必要になります。
つまり、AAVを用いたin vivoゲノム編集では、編集酵素が小型であることが大きな利点になります。小型であれば、ベクター内に必要な構成要素を収めやすくなり、設計の自由度が高まります。また、単一ベクター化の可能性が高まれば、製造、投与、品質管理、臨床開発の面でも利点が生まれます。
この観点から、近年注目されているのが、TnpBやIscBのような超小型RNA誘導型DNA編集酵素です。これらは、従来の代表的なCas酵素と比べて小型であり、AAVをはじめとする送達制約のある環境に適したツール候補として期待されています。
ただし、小型であることだけで医療応用に十分とは言えません。実際には、以下のような複数の条件を満たす必要があります。
- 標的DNA配列を十分に認識できること
- 目的部位で十分な編集活性を示すこと
- オフターゲットリスクを抑えられること
- 細胞内で安定して発現・機能すること
- 送達ベクターに適した構成にできること
- 用途ごとに設計変更できる余地があること
このため、超小型編集ツールの開発では、単に自然界から候補酵素を見つけるだけではなく、目的に合わせて配列や構造を最適化することが重要になります。
特に、標的配列の近傍に必要となるPAMまたはTAMの認識性は、編集可能な部位を大きく左右します。医療応用では、疾患原因変異や治療上重要なゲノム領域を狙う必要があります。そのため、編集酵素側の標的認識性やPAM/TAM制約を調整できることは、応用範囲を広げるうえで重要です。
AAVに搭載可能な超小型編集ツールは、単なる「小さい酵素」ではありません。それは、in vivoゲノム編集医療を現実の治療選択肢に近づけるための、送達設計と分子設計をつなぐ基盤技術です。
今後、ゲノム編集医療がより多くの疾患領域へ広がるためには、編集性能だけでなく、送達可能性を前提にしたツール開発が不可欠です。超小型編集ツールは、そのための重要な技術フロンティアの一つです。


