なぜ今、新しいゲノム編集ツールが必要なのか
- コラム
in vivoゲノム編集医療に残された「送達・サイズ・知財」の課題
ゲノム編集技術は、基礎研究から医療応用へと急速に広がっています。一方で、患者体内で直接ゲノムを編集するin vivo医療を実現するには、送達・分子サイズ・知財という現実的な制約を乗り越える必要があります。本記事では、なぜ今、新しいゲノム編集ツールが求められているのかを整理します。
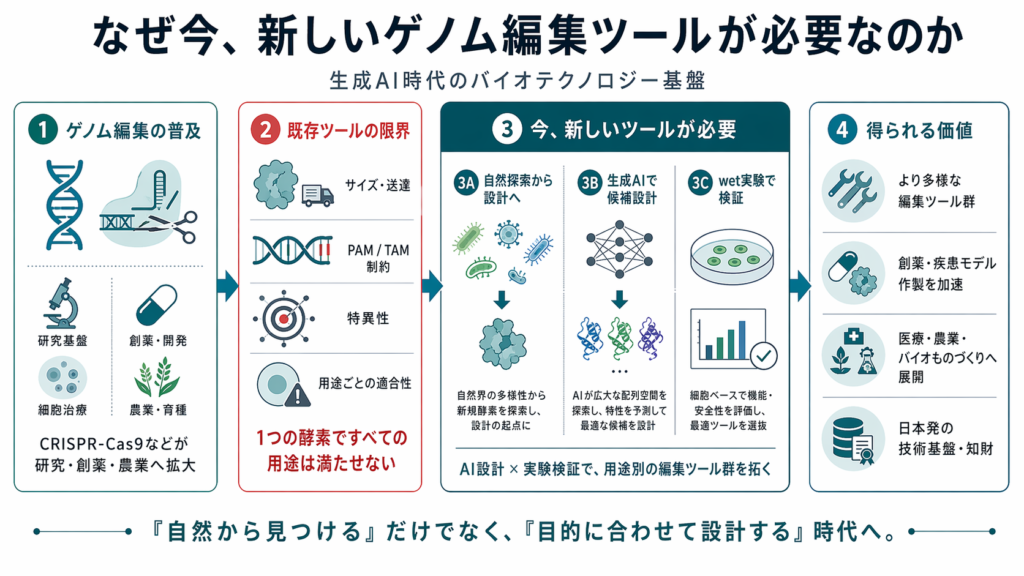
ゲノム編集技術は、この十数年で生命科学と医療のあり方を大きく変えてきました。CRISPR-Cas9をはじめとするRNA誘導型のゲノム編集技術により、従来は困難だった遺伝子改変を、比較的短期間かつ高い設計性をもって実行できるようになりました。
現在では、基礎研究だけでなく、細胞治療、遺伝子治療、疾患モデル作製、創薬研究など、さまざまな領域でゲノム編集技術の応用が進んでいます。特に、患者体内で直接ゲノムを編集する in vivoゲノム編集医療 は、これまで治療が難しかった遺伝性疾患や難治性疾患に対して、新しい治療選択肢を提供する可能性があります。
一方で、in vivoゲノム編集医療を本格的に広げていくうえでは、まだ重要な課題が残されています。代表的な課題が、送達、サイズ、知財 の3つです。
第一に、送達の課題です。ゲノム編集ツールは、標的となる臓器や細胞に正確に届けられなければ機能しません。現在、AAVベクターや脂質ナノ粒子などの送達技術が研究・開発されていますが、標的組織、投与経路、搭載できる分子サイズ、安全性、免疫応答などの制約があります。どれほど高性能な編集酵素であっても、体内の目的細胞に適切に届けられなければ、医療応用にはつながりません。
第二に、サイズの課題です。多くのゲノム編集酵素は分子サイズが大きく、送達ベクターに搭載する際の制約を受けます。特にAAVは、臨床応用で重要な送達手段の一つですが、搭載できる遺伝子サイズには上限があります。そのため、編集酵素、ガイドRNA、発現制御配列などを一つの設計に収めることが難しい場合があります。in vivo医療への展開を考えると、より小型で、送達しやすく、設計自由度の高い編集ツールが求められます。
第三に、知財の課題です。既存の代表的なゲノム編集技術は、強力である一方、知的財産の構造が複雑です。研究開発や事業化を進めるうえでは、技術性能だけでなく、どの技術空間を使うのか、どの用途で自由度があるのか、どのように独自性を確保するのかが重要になります。医療応用を目指す企業にとって、知財上の自由度は、研究開発戦略と事業戦略の両方に関わる重要な要素です。
このような背景から、現在注目されているのが、既存の大型ゲノム編集酵素だけに依存しない、新しい小型編集ツールの探索と設計です。近年、TnpBやIscBのような、よりコンパクトなRNA誘導型DNA編集酵素の研究が進んでおり、次世代のゲノム編集ツール候補として関心が高まっています。
これらの超小型編集ツールは、AAV搭載性、設計自由度、送達適性という観点から、in vivoゲノム編集医療における重要な技術基盤となる可能性があります。ただし、自然界に存在する酵素をそのまま使うだけでは、標的認識性、活性、安全性、編集効率などに課題が残る場合があります。したがって、自然探索と人工設計を組み合わせ、目的に応じた新しい編集ツールを開発することが重要になります。
今後のゲノム編集医療では、「既にある編集ツールをどう使うか」だけでなく、「目的に合わせてどのような編集ツールを設計するか」が問われる時代に入っていくと考えられます。
私たちは、送達・サイズ・知財という現実的な制約を踏まえながら、in vivoゲノム編集医療に適した新しい超小型編集ツールの開発可能性に注目しています。既存技術の延長だけでは届きにくい領域に対して、新しい分子設計のアプローチを取り入れることが、次世代のバイオ医療基盤につながると考えています。
- Jinek, M. et al. Science (2012). A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity.
- Cong, L. et al. Science (2013). Multiplex genome engineering using CRISPR/Cas systems.
- Ran, F. A. et al. Nature (2015). In vivo genome editing using Staphylococcus aureus Cas9.
- Wang, D., Tai, P. W. L., & Gao, G. Nature Reviews Drug Discovery (2019). Adeno-associated virus vector as a platform for gene therapy delivery.


